تحریریه پزشك امروز
سلاح جدیدی برای مقابله با سرطان
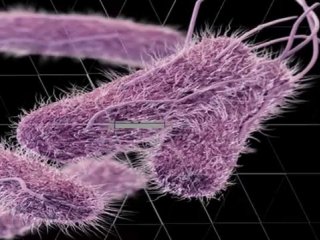
محققان به تازگی اعلام كردند كه میكروب سالمونلا سلاح جدیدی برای مقابله با سرطان است. یك پژوهش جدید نشان داد سالمونلا سیستم دفاعی خود بدن را در مقابل بیماری قرار میدهد. دانشمندان كشف كردهاند كه درمان تومورهای سرطانی با باكتری سالمونلا میتوانند سبب ایجاد یك واكنش ایمنی شود كه بهطور موثر سلولهای سرطانی را نابود میسازد و همچنین در برابر رشد بیشتر تومورها، بدن را واكسینه میسازد.
سلولهای سرطانی بهویژه خطرناك هستند چون سیستم ایمنی بدن را میتوانند از كار بیاندازند. درمان این سلولهای سرطانی با سالمونلا باعث میشود كه تومور برای سلولهای سیستم دفاعی بدن قابل رویت شود و بنابراین سیستم دفاعی به سلولهای سرطانی حملهور میشود.
مرجانهای رنگارنگ دریایی، امید دیگری برای درمان سرطان
دانشمندان میگویند، مرجانهای رنگارنگ در كف دریاها، امید دیگری برای درمان سرطان هستند. این تخته رنگهای مرجانی در كف اقیانوسها كه جوامع نادر با خاصیت فلورسنت بالا هستند، علاوه بر خاصیت مقابله با گرمای جهانی، برای درمان سرطان هم میتوانند مفید باشند.
آینا صالح، پژوهشگر دانشگاه غرب سیدنی از رنگدانههای حاصل از این مرجانها استفاده كرده تا برچسبهای فلورسنت جدیدی را تولید كند كه به ردیابی عملكرد درونی سلولی و كشف مشكلاتی كه منجر به سرطان میشوند، كمك خواهد كرد. دكتر صالح میگوید مرجانهای قرمز برای این منظور بیشتر مورد استفاده دارند چون به محققان امكان میدهند كه نقاط عمیقتری را در درون بافتها ببینند. محققان تصریح كردند، این كشف دلیل دیگری است كه توجیه میكند چرا حفظ تنوع زیستی تا این حد حائز اهمیت است.
ساخت خون مصنوعی با کمک سلولهای بنیادین جنینی
دانشمندان انگلیسی موفق شدند سلولهای بنیادین به جا مانده از تکنیک IVF را در راستای پروژهای به منظور تولید انبوه تجاری خون مصنوعی به گلبولهای قرمز تبدیل کنند. این اولین باری است که در انگلستان محققان توانستهاند از سلولهای بنیادین جنینی سلولهای خونی تولید کنند. هدف این پروژه سه میلیون پوندی ایجاد منبع جایگزین از گروه خون O منفی است، تنها گروه خونی جهانی که میتوان بدون واهمه از پسزدگی آن را به هر گروه خونی دیگری انتقال داد.
در این پروژه از بیش از صدها سلول بنیادین جنینی به جا مانده از کلینیکهای باروری در خطوط متعدد تولید سلولهای بنیادین که میتوان آنها را در محیط آزمایشگاهی بارها بازتولید کرد استفاده شده است. در یکی از این خطوط تولیدی به نام RC-7 سلولهای بنیادین جنینی قبل از تبدیل شدن به سلولهای خونی کاربردی که پروتئین حامل اکسیژن هموگلوبین را به همراه دارند، به سلولهای بنیادین خونی تبدیل میشوند.
به گفته محققان ساخت خون مصنوعی در ابعاد تجاری میتواند بر بسیاری از مشکلات موجود ناشی از کمبود خون و خطر احتمال انتقال عفونت و آلودگی از اهداکننده به گیرنده غلبه کند. در صورتی که همه چیز طبق برنامه پیش رود تا پنج سال آینده امکان آغاز اولین دور از آزمایشهای خون مصنوعی ساخته شده از سلولهای بنیادین جنینی به وجود خواهد آمد. پس از آن هدف نهایی افزایش میزان تولید به منظور تولید سالانه دو میلیون واحد خواهد بود.
ترمیم ضایعات قلب و نخاع با ماكارونیهای سلولی!
محققان در ایالات متحده، موفق به ساخت رشتههای ماکارونی مانندی حاوی سلولهای زنده شده اند که به آنها سیمهای سلولی میگویند. این کار خود گامی جلو در درمان است و با استفاده از نتایج این تحقیق میتوان بافت قلب و نخاع را ترمیم و یا حتی عضلات مصنوعی طراحی کرد.
سام استاپ یکی از محققان در دانشگاه نورثوسترن میگوید: «روشی را کشف کردهایم تا با کمک آن، آرایههای بزرگی از فیلامانهای در حد نانو و سلولهای زنده در فواصل ماکروسکوپیک را تعیین راستا کنیم. این آرایهها، ژل ماکارونی مانندی را تشکیل میدهند که قابلیت پیوند شدن به بافتهای قلبی یا عصبی را در راستاهای سلولی را داراست.»
برای ساخت این رشتهها، گروه استاپ محلولی از پپتیدهای آمفیفیلیک را که میتوانند به صورت دستجاتی از نانوالیاف خودآرایی شوند، در نظر میگیرند. این محلول برای بلور شدن گرم میشود و سپس با کمک یک پیپت فشردهشده به درون آب نمکی ریخته میشود که حاوی کلرید سدیم یا کلرید کلسیم است.
استاپ شرح میدهد: «زمانی که بلور مایع با دست روی واسط نمکی ریخته میشود، تمامی محتوا در یک جهت قرار میگیرند و یونهای کلسیم راستا را به شکل یک ژل ماکارونیمانند، منجمد میکنند. رشتههای حاصله غیرسمی بوده، میتوانند روی هم انباشته و یا رول شوند و با تغییر قطر پیپت میتوانند ضخامت متفاوتی را داشته باشند.
در مرحله بعد، گروه، سلولهای بنیادی را به محلول پپتیدی اضافه کرد. این سلولها توانستند سنتز خود را حفظ کرده، در ساختار گیر بیفتند. مشاهده شد که سلولها در ساختار کثرت پیدا میکنند و در جهتهای یکسانی رشد میکنند. هونگبین لی- محققی که اخیرا در دانشگاه بریتیش کلمبیا در ونکوور کانادا پروتئینهای مصنوعی را طراحی کرده که مشابه بافت عضله هستند- میگوید: «این کار نشان میدهد که گامی مهم بهسوی ساخت ماهیچههای مصنوعی برداشته شده است.» او اضافه میکند: «این کار همچنین نشان میدهد که داربست (اسکافولد) مهندسی بافت جدید، ممکن است به ترمیم عضله یا عصب آسیبدیده در بیماران کمک کند.»