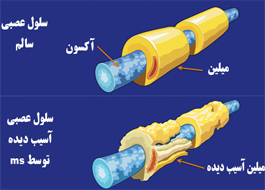
عوامل اصلی ايمونولوژيك در بيماری مولتيپل اسكلروزيس
در شماره قبلی درخصوص اتیولوژی و مكانیزم ایجاد بیماری مولتیپل اسكلروز صحبت شد.
شواهد دخالت سلولهای TCD4+ در MS
پس از شرح بیماری MS توسط شاركوت در سال 1868 و مشاهدات پاستور در زمینه انسفالومیلیت حاد متعاقب واكسیناسیون در خرگوشها. در سال 1933، ریورز نشان داد كه تزریق هموژنه نخاع یا مغز به پریماتهای سالم باعث بیماری شبه MS میشود. لذا این تصور شكل گرفت كه MS یك بیماری خود ایمن است.
اگرچه این یك باور ابتدایی است، با این حال شواهد موجود در زمینه پیشرفت MS هنوز موید آن است كه سلولهای TCD4+ ضدخودی در پاتوژنز MS نقش محوری ایفا میكنند.
از جمله دلایل موجود به موارد زیر میتوان اشاره نمود:
1- سلولهای TCD4+ به عنوان سلولهای التهابی به CNS و CSF بیماران MS ارتشاح پیدا میكنند.
2- خطر ابتلاء ژنتیكی به وسیله مولكولهای HLA-DR و HLA-DQ به ارث میرسد.
3- موشهای ترانس HLA-DR یا HLA-DQ به EAE حساس میباشند.
4- تولید آنتیبادی، بلوغ سلولهای CD8+ و بسیاری از فعالیتهای ایمنی اكتسابی و ذاتی، حداقل تا حدودی به وسیله سلولهای Th CD4+ كنترل میشود.
ارتباط HLA با عملكرد سلولهای TCD4+
عملكرد اغلب سلولهای TCD4+ اختصاصی میلین به مولكولهای HLA-DR و موارد نادری به مولكولهای DP, DQ وابستهاند. از آنجایی كه HLA-DP5 با MS نوع آسیایی همراه است، این ذهنیت كه در این بیماری واكنشهای مهمی بین مولكولهای HLAfailed كلاس II، پاسخ سلولهای T و ویژگیهای بیماری اتفاق میافتد را تقویت میكند. اطلاعات موجود حاكی از آن است كه در این شرایط سلولهای T به سمت تمایز به Th1 سیر میكنند.
علیرغم اینكه هیچ یك از سلولهای MS مولكول HLAII را بروز نمیدهند، لیكن سلولهای TCD4+ به طور غیرمعمول اولیگودند روسیتها (و ندرتا سلولهای عصبی) را به طور مستقیم لیز میكنند.
در MS واكنش CD80/CD86 روی APC با CD28 سلولهای T و پیام منفی CTLA-4 سلولهای T مختل میباشد.
سلولهای TCD4+ اختصاصی میلین (نظیر سلولهای T ضد سایر آنتیژنها) یا به، كمك محركها وابسته نیستند یا وابستگی كمتری دارند، همچنین به CTLA-4، یا پاسخ نمیدهند یا كمتر پاسخ میدهند. حالت اخیر به خاطر فقدان CTLA-4 در سطح سلولهای CD28 TCD4+ است.
سلولهای تحت كنترل Th2 نظیر ماست سلها نیز در تخریب بافت نقش دارند.
از نظر گنجینه TCR نیز بررسیهای اولیه حاكی از آن است كه در برخی مدلهای حیوانی، گنجینه TCR بسیار كم و محدود است.
سلولهای TCD8+
نه تنها در بیماری MS بلكه در سایر بیماریهای خودایمن نیز اطلاعات بسیار كمی در مورد سلولهای TCD8+ نسبت به سلولهای TCD4+ وجود دارد. شاید مشكلات تكنیكی و عملی در مطالعه این سلولها یكی از دلایل این امر باشد. با این حال به دلایل زیر در CNS سلولهای TCD8+ از نظر نقش و عملكرد بیشتر مورد بررسی قرار گرفتهاند.
1- به جز میكروگلیاها هیچ یك از سلولهای CNS مولكولهای MHCII را بارز نمیكنند. این مولكولها تحت تاثیر IFN-y بر روی آستروسیتها (نه اولیگودندروسیتها یا نرونها) ظاهر میشوند. لذا سلولهای اخیر تنها توسط سلولهای TCD8+ شناسایی میشوند.
2- حضور سلولهای TCD8+ در CSF و خون محیطی و تكثیر دائم اولیگوكلونال سلولهای خاطرهای CD8+ در CSF و بافت مغزی بیماران MS.
3- سلولهای TCD8+ در بافت مغز مبتلایان به MS بسیار فراوانتر از سلولهای TCD8+ است.
4- بر روی سلولهای عصبی معیوب، MHCI ظاهر میشود و سلولهای TCD8+ اختصاصی ویروس میتوانند از طریق سیتولیز به واسطه fas/FasL مستقیما باعث مرگ سلول شوند.
5- مقداری از اپیتپهای میلین منحصر به HLA-I در MBP، PLP، MAG و... مشخص شده و در بیماران MS پاسخ سلولهای TCD8+ سیتوتوكسیك به MBP افزایش نشان میدهد.
6- سلولهای TCD8+ اختصاصی میلین IL-16 و IP-10 ترشح میكند كه برای سلولهای TCD4+ اختصاصی میلین كوتاكتیك هستند.
7- سلولهای TCD8+ اختصاصی اپیتپ MBP در موشهای وحشی C3H آنسفالیتزا بوده و بیماری شبه MS (به ویژه از نظر آتاكسی) ایجاد میكنند. در حالی كه سلولهای TCD4+ مدلهای EAE را به وجود میآورند.
8- افزایش تولید لنفوپویتین در بیماران SP-MS، افزایش میزان چسبندگی به سیاهرگهای مغز، افزایش میزان سلولهای TCD8 ضد اپیتپهای EBV و ارتباط بین تولید سیتوكاینها و تولید سلولهای TCD8+ و تخریب بافتی قابل مشاهده در MRI، از دیگر دلایل نقش این سلول در MS است.
لنفوسیتهای B و آنتیبادیها
مهمترین و ابتداییترین دلیل بر نقش لنفوسیتهای B و آنتیبادیها در پاتوژنز MS، افزایش ایمونوگلوبولینها در CSF این بیماران است. سلولهای B نمیتوانند از سدخونی- مغزی عبور كنند. با این حال با شروع التهاب، این سلولها همراه آنتیبادیها و كمپلمان وارد CNS میشوند. افزایش ایمونوگلوبولینها در CSF بیماران (نه در سرم) بیانگر تولید موضعی آن است.
لنفوسیتهای B و آنتیبادیها به طرق مختلف به شرح زیر در پاتوژنز MS نقش دارند:
1- این سلولها میتوانند به عنوان APC برای سلولهای T ضدخودی عمل كنند.
2- اینها میتوانند كمك محرك لازم برای سلولهای T ضدخودی را فراهم آورند.
3- سلولهای T و آنتیبادیهای موجود در بافت موجب فراخوان سلولهای T ضدخودی به CNS میشوند.
4- سلولهای T اختصاصی ایدیوتیپ ممكن است به وسیله آنتیبادیهای CSF فعال شده و سلولهای Bای كه این ایدیوتیپها را تولید میكنند، مورد حمایت قرار دهند.
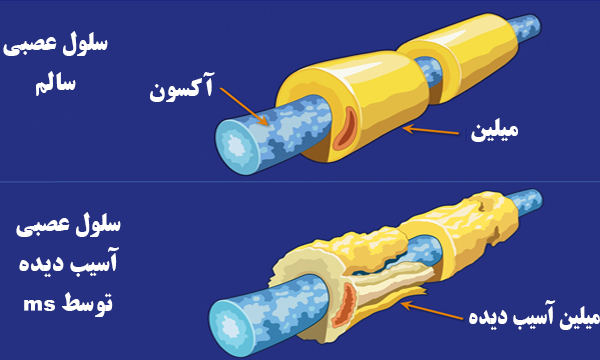
5- تولید آنتیبادی ضد میلین و تخریب میلین داخل پلاكها مهمترین طریق ایفای نقش سلولهای B در پاتوژنز بیماری است.
در سال 1959 محققین با نشان دادن فعالیت میلینزدایی یك فاكتور سرمی (كه بعدها مشخص شد آنتیبادی اختصاصی میلین است)، نشان دادند كه فاكتورهای هومورال میتوانند در دمیلینه نمودن التهابی ایفای نقش كنند. بررسی هیستو پاتولوژیك CNS و آنالیز CSF نیز این موضوع را تایید نمود.
در پلاكها و نواحی دمیلینه فعال MS، سلولهای B، پلاسما سلها و آنتیهای اختصاصی میلین شناسایی شدهاند. آنتیبادیها با اسپونیزه كردن میلین موجب فاگوسیته شدن آن و با فعال كردن كمپلمان و واكنش سیتولیز باعث از بین رفتن میلین میشوند.
تاثیر پاتوژنیك آنتیبادی اختصاصی MBP در EAE مشخص نشده و در مورد MS نیز اختلال نظر وجود دارد. در CSF بیماران MS افزایش تعداد لنفوسیتهای B مولد آنتیبادی ضد PLP نشان داده شده و آنهایی كه پاسخ دائم ضد PLP دارند، از آنهایی كه آنتیبادی ضد MBP دارند، قابل تمیز میباشند.
آنتیبادی ضد اجزاء فرعی میلین نیز شناسایی شده است. MOG مهمترین اتو آنتی ژن هدف سلولهای B در MS است. برخلاف آنتیبادی ضد MBP یا PLP، آنتیبادی ضد MOG در EAE قادر به تخریب میلین است. آنتیبادی ضد MOG در جراحات MS نیز یافت شده است.
در MS پاسخ سلول B به MOG افزایش نشان میدهد. آنتیبادی سرمی ضد MOG در بیماران با علائم اولیه CNS و علائم MRI، بیانگر عود قطعی MS است.
نكته جالب اینكه آنتیبادیها از دو طریق ممكن است نقش مفید ایفا كنند. اول اینكه ممكن است باعث تولید سیتوكاینهای Th2 شوند. دوم اینكه آنتیبادی ضد برخی اجزاء CNS میتواند التیام میلین را تسریع كند.
در مدلهای حیوانی MS، IgM ضدبرخی آنتیژنهای CNS باعث افزایش بازسازی میلین میشود.
شواهد دیگر دال بر نقش مفید آنتیبادیها در درمان MS، استفاده از IVIG است كه از طرق مختلف از جمله مهار رسپتور FC، غیرفعالسازی سیتوكاینها، مهار كمپلمان، مهار CD4 و MHC، و تعدیل آپوپتوز در درمان این بیماری مرموز ایفای نقش میكند.